 Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Chemieklausuren, Arbeitsblätter und mehr: www.deinchemielehrer.de
Aufgabensammlung für das Fach Chemie in der Schule
Aufgaben mit Lösung: Elektrochemie
Alle Aufgaben mit LösungElektrochemieOrganische Chemie
Übersicht - ElektrochemieElektrolyse einer O,1mol/l Kupfersulfat-lösung an Kupfer- und an Platinelektroden Elektrochemische Bestimmung des Löslichkeitsproduktes von Silberchlorid AgClElektrochemische Bestimmung des Löslichkeitsproduktes von Silberbromid AgBr
Zur Bestimmung des Löslichkeitsproduktes von Silberbromid AgBr baut man ein galvanisches Element auf.
Die erste Halbzelle besteht aus einer Standardwasserstoffhalbzelle, die zweite aus einer 0,1 mol/l AgNO3-Lösung, in die eine Silberelektrode taucht.
Zu dieser zweiten Lösung wird jetzt eine 0,1 mol/l KBr-Lösung zutitriert. Dabei wird die Spannung in Abhängigkeit von dem Volumen der zutitrierten KBr-Lösung gemessen. Man beobachtet, dass mit der Zugabe der KBr-Lösung festes AgBr ausfällt.
Folgende Werte der gemessenen Spannung in Abhängigkeit von der zutitrierten KBr-Lösung werden aufgenommen:
0,1 mol/l KBr (ml) | U (V) |
0 | 0,751 |
1 | 0,748 |
2 | 0,745 |
3 | 0,743 |
4 | 0,740 |
5 | 0,738 |
6 | 0,735 |
7 | 0,732 |
8 | 0,729 |
9 | 0,726 |
10 | 0,722 |
11 | 0,719 |
12 | 0,715 |
13 | 0,711 |
14 | 0,706 |
15 | 0,701 |
16 | 0,694 |
17 | 0,686 |
18 | 0,675 |
19 | 0,657 |
20 | 0,447 |
21 | 0,238 |
22 | 0,221 |
23 | 0,211 |
24 | 0,204 |
25 | 0,199 |
26 | 0,195 |
27 | 0,192 |
28 | 0,189 |
29 | 0,186 |
30 | 0,184 |
Aufgaben
a) Zeichnen Sie den Versuchsaufbau und beschriften Sie die Zeichnung..
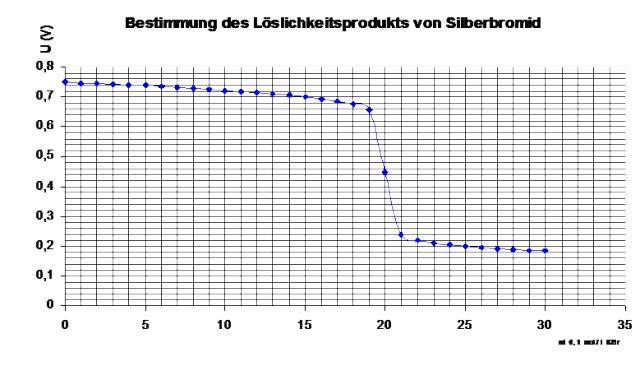
b) Stellen Sie die aufgenommenen Messwerte graphisch dar und beschreiben Sie die Aussage der graphische Darstellung.
c) Erläutern und begründen Sie aus den Gesetzmäßigkeiten der Elektrochemie die Entstehung der gemessenen Spannung.
d) Leiten Sie ausgehend vom Massenwirkungsgesetz das Löslichkeitsprodukt für das Salz AgBr ab. Zeigen Sie auf, welche Vorgänge bei der Zugabe des KBr-Titers in der Lösung ablaufen und begründen Sie so den Verlauf des Graphen.
e) Bestimmen Sie das Löslichkeitsprodukt aus den experimentell aufgenommenen Daten. Begründen Sie Ihre Berechnung.
Nomalpotentiale
reduzierte Form | Oxidierte Form | Eo (V) |
Li | Li+ +e- | -3,03 |
Ca | Ca2+ + 2e- | -2,76 |
Na | Na+ + e- | -2,71 |
Al | Al3+ +3e- | -1,69 |
Zn | Zn2+ + 2 e- | -0.76 |
Fe | Fe2+ + 2 e- | -0,44 |
Pb | Pb2+ + 2 e- | -0,13 |
H2 + 2 H2O | 2 H3O+ + 2 e- | 0,00 |
Cu | Cu2+ + 2e- | +0,35 |
4 OH- | O2 + 2 H2O + 4 e- | +0,40 |
Fe2+ | Fe3+ + e- | +0,75 |
Ag | Ag+ + e- | +0,81 |
2 Cl - | Cl2 + 2e- | +1,36 |
Au | Au3+ + 3e- | +1,38 |
12 H2O + Mn2+ | MnO4- + 8H3O+ + 5e- | +1,50 |
2 SO42- | S2O82- + 2e- | +2,05 |
2 F- | F2 + 2e- | +2,85 |
Lösung
a) Anfertigung einer Zeichnung des Versuchsaufbaus.
b) Graphische Darstellung der Messwerte und Beschreibung der Aussage des Graphen
c) Das hier gezeigte galvanische Element ist das Redoxsystem H2+2H2O/2H3O+//Ag/Ag+. Die Silberhalbzelle bildet den +Pol. Diese Erkenntnis führt in Anwendung der Theorie der Erlektrochemie zur Darlegung und Interpretation der Begriffe Lösungsdruck und Abscheidungsdruck im Zusammenhang mit der Potentialbildung bzw. der gemessenen Spannung. So gelangt man zur Erklärung der sinkenden Spannung des Elementes bei Zutitration der KBr und der damit verbundenen Senkung der Konzentration der Silberionen.
d) Ableitung des Löslichkeitsproduktes aus dem Massenwirkungsgesetz und Erklärung der in der Lösung ablaufenden Vorgänge: Bei Zugabe des Titers KBr fällt AgBr kontinuierlich aus. Entsprechend verringert sich die Konzentration an Ag+ - Ionen und somit sinkt die Spannung.
In der Nähe des Äquivalenzpunktes ist die Konzentration der noch in der Lösung verbliebenen Ag+-Ionen klein im Vergleich zur Menge der zugegebenen Br--Ionen, was letztlich eine relativ große Änderung der Konzentration der Silberionen zur Folge hat. Damit ändert sich die Spannung im Vergleich zu den vorhergehenden Schritten relativ stark, wodurch sich der charakteristische Verlauf der Kurve erklärt.
e) Am Äquivalenzpunkt der aufgenommenen Titrationskurve liegt eine äquimolaren Lösung von Ag+ und Br- Ionen vor. An diesem Punkt misst man eine Spannung von 0,447 V. Damit gilt an diesem Punkt:
0,81 = 0,447 + 0,059 * log c (Ag+)
C(Ag+) = 7* 10 –7
Daraus folgt, da c(Ag+) = c(Br-) ist
KL = (7* 10 –7)2
KL = 7 * 10 - 14
E= 0,81 +0,059 + log 7* 10 –7
E = 0,447 V
Dieses Potential ist aus dem Graphen am Äquivalenzpunkt abzulesen. Es berechnet sich dann entsprechend der obigen Rechnung durch Einsetzen in die Nernst’sche Gleichung umgekehrt die Konzentration der Silberionen und daraus wieder der Wert für das Löslichkeitsprodukt.
Matthias Rinschen (C) 2006 - 2024, Mail: deinchemielehrer [at] gmx [dot] de, Impressum und Datenschutzerklärung